Pourquoi les dispositifs médicaux fabriqués en Europe sont plus importants que jamais

L’UE interdit aux entreprises chinoises d’accéder à des contrats médicaux de grande valeur
Le 20 juin 2025, la Commission européenne a officiellement interdit aux entreprises chinoises de soumissionner pour des appels d’offres portant sur des dispositifs médicaux d’une valeur supérieure à 5 millions d’euros, invoquant un accès déloyal en Chine et des pratiques discriminatoires en matière de passation de marchés. Cette mesure concerne 60 % de la valeur des marchés publics de l’UE et marque la première application de l’Instrument relatif aux marchés publics internationaux (IPI) – une déclaration forte en faveur de la concurrence loyale et de la souveraineté dans le domaine de l’approvisionnement en soins de santé.
Ce que cette évolution signifie pour les hôpitaux et les équipes chargées des achats
- L’Union européenne fait pression pour que les fournisseurs soient locaux et de confiance.
- Les décisions d’approvisionnement ne sont plus seulement une question de prix, mais aussi de sécurité, de transparence et de contrôle.
- Les dispositifs médicaux fabriqués dans l’UE présentent désormais des avantages stratégiques et financiers dans les appels d’offres à grande échelle.
Pourquoi il est important que nous fabriquions aux Pays-Bas et en France 🇳🇱🇫🇷
1. Des chaînes d’approvisionnement plus courtes = un traitement plus rapide
En produisant en France et aux Pays-Bas, TSC Life assure une disponibilité constante des produits sans goulots d’étranglement au niveau de l’expédition internationale. Dans un secteur où le timing est critique, la production locale garantit la rapidité et la fiabilité.
2. Conformité totale aux normes CE et MDR de l’UE
Nos appareils sont entièrement conformes à la réglementation européenne sur les dispositifs médicaux (MDR) et portent la marque CE, ce qui signifie qu’ils répondent aux normes de sécurité, de performance et de qualité les plus strictes d’Europe. Aucun besoin de recertification ou d’interprétation – ils sont prêts à l’emploi.
3. Accès aux mesures d’incitation et aux prix préférentiels français
Le plan d’innovation santé 2030 de la France encourage les dispositifs médicaux fabriqués dans l’UE par le biais d’outils tels que les crédits de prix du CSIS, qui récompensent l’innovation et la production locales. Les acheteurs de nos produits peuvent bénéficier d’avantages tarifaires et d’un alignement des remboursements lorsqu’ils choisissent des dispositifs fabriqués en France.
4. Profiter de la croissance des technologies médicales en Europe
Le marché européen des dispositifs médicaux est le deuxième plus grand au monde et devrait passer de 140 milliards de dollars en 2022 à 171 milliards de dollars d’ici 2027. L’externalisation au sein de l’UE – en particulier vers des fabricants de confiance en France et aux Pays-Bas – augmente rapidement. Le marché de l’externalisation de l’UE a atteint 30,4 milliards de dollars en 2024 et croît à un taux de croissance annuel moyen de plus de 12 %.
5. Moins de risques réglementaires et géopolitiques
Avec la montée des tensions commerciales, des droits de douane et des contrôles à l’exportation, il est de plus en plus risqué de s’approvisionner en dehors de l’UE. En revanche, les fournisseurs établis dans l’UE offrent une clarté juridique, une stabilité et des avantages stratégiques à long terme.
Comment TSC Life met en avant la valeur de l’UE
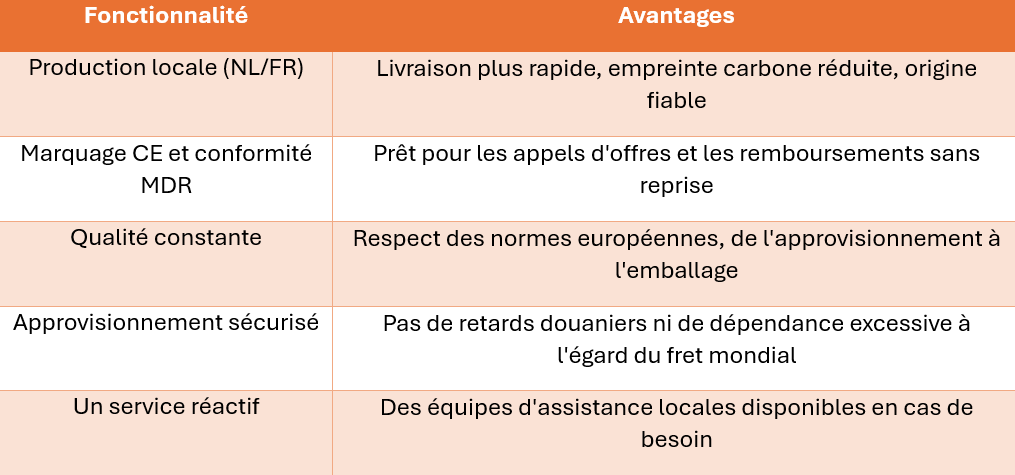
Les marchés publics évoluent. Choisissez un partenaire déjà en phase avec l’avenir.
Références
- EU bars Chinese firms from most medical device tenders – Reuters, June 20, 2025
https://www.reuters.com/business/healthcare-pharmaceuticals/eu-bars-chinese-firms-most-medical-device-tenders-2025-06-20 - EU restricts Chinese medical devices in new trade dispute – Financial Times, June 20, 2025
https://www.ft.com/content/ef82222b-f616-493a-b863-59adb40e68d5 - EU spurns economic dialogue with China over deepening trade rift – Financial Times, June 21, 2025
https://www.ft.com/content/81700fc4-8f23-4bec-87e9-59a83f215431 - International Procurement Instrument (IPI) – European Commission
https://policy.trade.ec.europa.eu/international-procurement-instrument_en - Medical Devices Regulation (EU MDR) – European Medicines Agency (EMA)
https://www.ema.europa.eu/en/human-regulatory/overview/medical-devices - Health Innovation Plan 2030 – French Ministry of Health (Ministère de la Santé)
https://solidarites-sante.gouv.fr/actualites/presse/dossiers-de-presse/article/health-innovation-plan-2030 - European MedTech Market Outlook 2022–2027 – MedTech Europe
https://www.medtecheurope.org - EU Medical Device Outsourcing Market Report 2024 – ResearchAndMarkets.com
https://www.researchandmarkets.com/reports/5795462/europe-medical-device-outsourcing-market